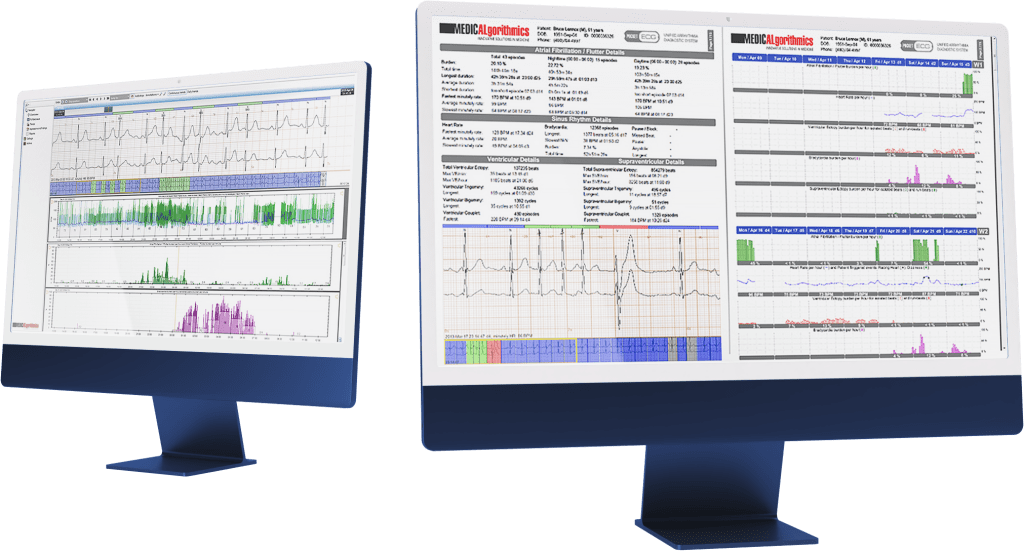
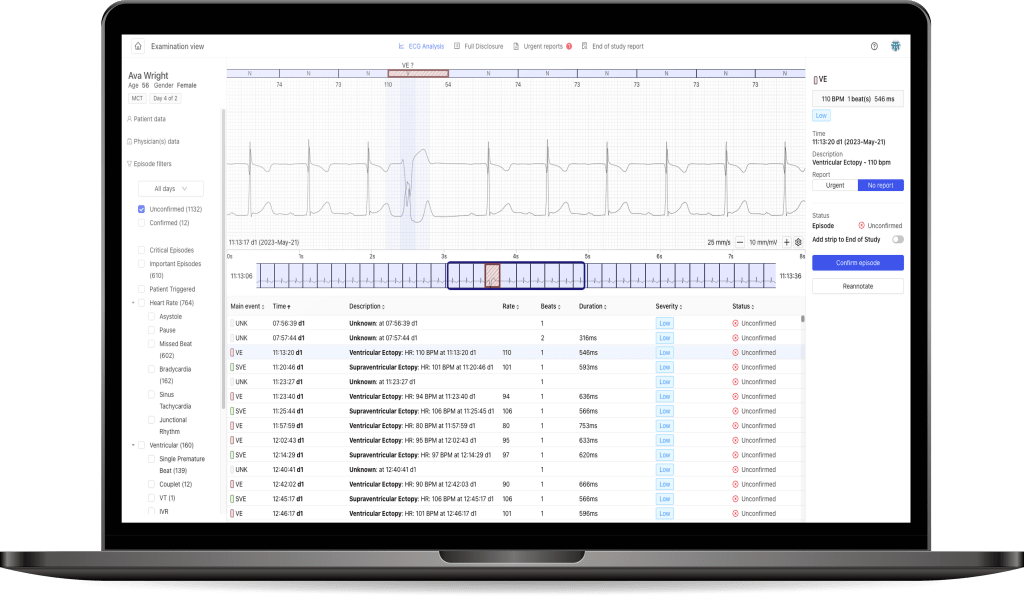
Medicalgorithmics został wybrany przez firmę CRO Simbec-Orion jako dostawca rozwiązań do zdalnej diagnostyki w badaniu klinicznym na zlecenie spółki biotechnologicznej Molecure. W badaniu z użyciem urządzenia PocketECG IV i chmurowego rozwiązania PC Client weźmie udział około 90 pacjentów w ośrodkach badawczych w Europie i USA.
„Cieszymy się, że renomowana, międzynarodowa firma CRO dostrzegła wartość w jakości diagnostycznej i elastyczności naszych rozwiązań do monitoringu bezpieczeństwa kardiologicznego. To kolejne potwierdzenie, że nasza technologia jest przydatna nie tylko w codziennej diagnostyce pacjentów, ale również w badaniach klinicznych nad potencjalnie nowymi lekami” – mówi Magdalena Ślusarczyk, dyrektor ds. klinicznych i wdrożenia produktów w Medicalgorithmics i dodaje „Warto odnotować, że po raz pierwszy w badaniach klinicznych pacjenci zostaną przebadani najnowszą wersją naszego urządzenia PocketECG IV, które będzie wykorzystywane do kardiologicznej kontroli zapisu reakcji na inhibitor. Udział w badaniach klinicznych wpisuję się w naszą nową strategię rozwoju i otwiera nam drogę do udziału w kolejnych badaniach realizowanych przez polskie i zagraniczne podmioty biotechnologiczne” – podsumowuje Magdalena Ślusarczyk.
Biotechnologiczna spółka Molecure przygotowuje się do rozpoczęcia badania klinicznego fazy II typu Proof-of-Concept w celu określenia skuteczności klinicznej oraz bezpieczeństwa inhibitora chitynaz OATD-01 u pacjentów z aktywną sarkoidozą płucną. Cząsteczka OATD-01, która w 2020 r. ukończyła I fazę badań klinicznych, jest podwójnym inhibitorem chitynaz. Chitynazy odgrywają kluczową rolę w procesach zapalnych i włóknieniowych obserwowanych m. in. w sarkoidozie. Związek OATD-01 jest pierwszym na świecie potencjalnym lekiem wykorzystującym mechanizm blokowania chitynaz.
Celem badania klinicznego fazy II jest określenie skuteczności klinicznej, farmakokinetyki, farmakodynamiki oraz bezpieczeństwa inhibitora chitynaz OATD-01 u pacjentów z aktywną sarkoidozą płucną. Będzie to badanie kliniczne fazy II, ze stałą dawką podawanego związku. Badanie zostanie przeprowadzone z udziałem około 90 pacjentów w ośrodkach badawczych w Europie i Stanach Zjednoczonych. Molecure przewiduje, że rozpoczęcie badania oraz włączenie pierwszego pacjenta nastąpi w IV kwartale 2023 r. Pacjenci uczestniczący w badaniu będą monitorowani technologią Medicalgorithmics przez około 6 tygodni pod kątem ewentualnego wystąpienia arytmii serca.
Medicalgorithmics po raz kolejny w tym roku został wybrany do udziału w międzynarodowych badaniach klinicznych. W kwietniu br. AnaCardio (szwedzka firma biofarmaceutyczna) wybrała Medicalgorithmics na dostawcę sprzętu do monitorowania bezpieczeństwa kardiologicznego (PocketECG III) w badaniu klinicznym GOAL-HF1. To podwójnie randomizowane i podwójnie zaślepiane badanie kliniczne fazy Ib/IIa eskalacji dawki i ekspansji kohorty, prowadzone u pacjentów z niewydolnością serca i obniżoną frakcją wyrzutową lewej komory (HFrEF).